Max-Eder Nachwuchsgruppe für Molekulare Immuntherapie (Müller)
- CAR T Zelltherapie bei malignen und autoimmunen Erkrankungen
- Zielgerichtete Therapien im Immunkompetenten System und deren Langzeitwirkung auf das Immunsystem
- Neue CAR T Zellbasierte Therapiekonzepte
Mitarbeiter
- PD Prof. Dr. med. habil. Fabian Müller, Arbeitsgruppenleiter
- Dr. rer. nat. Franziska Gsottberger, Post-Doc
- Dr. rer. nat. Hao Yao, Post-Doc
- Dr. med. Julia Katharina Scholz, Physician Scientist
- Dr. med. Isabel Korte, Clinician Scientist
- Giulia Benintende, MD PhD graduate program
- Alessia Crocione, graduate student
- Lisa Steger, cand. med.
- Lisa Mellenthin, V-MTLA
- Srdjan Petkovic, MTLA
Forschungsschwerpunkt
Zelltherapie gehört zu den bemerkenswertesten Errungenschaften der modernen Hämatologie und Onkologie. Als „lebendes Medikament“ gibt sie Patientinnen und Patienten mit zuvor unheilbaren Erkrankungen – darunter Krebs und Autoimmunerkrankungen – neue Hoffnung und könnte künftig auch die Behandlung von Infektionen oder von erblichen Erkrankungen unterstützen.
Dennoch steht die Zelltherapie weiterhin vor zahlreichen Herausforderungen. Dazu zählen unter anderem ungünstige Mikroumgebungen lokal am Krebs selbst, die eine optimale Funktion der Zellen verhindern können. Darüber hinaus fehlen bislang verlässliche Biomarker, um vorherzusagen, welche Patientinnen und Patienten mehr als nur CAR-T-Zellen der zweiten Generation benötigen, ob definierte zusätzliche Interventionen in einer bestimmten Mikroumgebung erforderlich wären oder wie sich Zelldynamik und Entzündungszustand eines Patienten funktionell auf expandierende und infiltrierende CAR-T-Zellen im Tumormikromilieu auswirken.
Aufbauend auf unserer Erfahrung im Bereich B-zellgetriebener entzündlicher Autoimmunerkrankungen und den neuen Erkenntnissen zum Immunsystem von Lymphompatienten untersuchen wir diese Fragestellungen aus verschiedenen Perspektiven. Dazu gehört das Verständnis der durch Lymphome ausgelösten Entzündung und ihrer vielfältigen Auswirkungen auf Zelltherapien, die gezielte und krankheitsspezifische Modulation dieser Entzündung sowie die Nutzung dieser neuen Erkenntnisse zur Verbesserung der CAR-T-Zelltherapie in vollständig immunkompetenten In-vivo-Modellen aggressiver und indolenter Lymphome. Im Einklang mit dem zentralen Laborthema – dem Verständnis von Resistenzmechanismen gegenüber Immuntherapien durch translationale Forschung – verfolgen wir das Ziel, Therapien zu verbessern und damit die Behandlungsergebnisse unserer Patientinnen und Patienten in der Hämatologie, Rheumatologie, Gastroenterologie sowie weiteren aufkommenden Krankheitsentitäten nachhaltig zu verbessern.
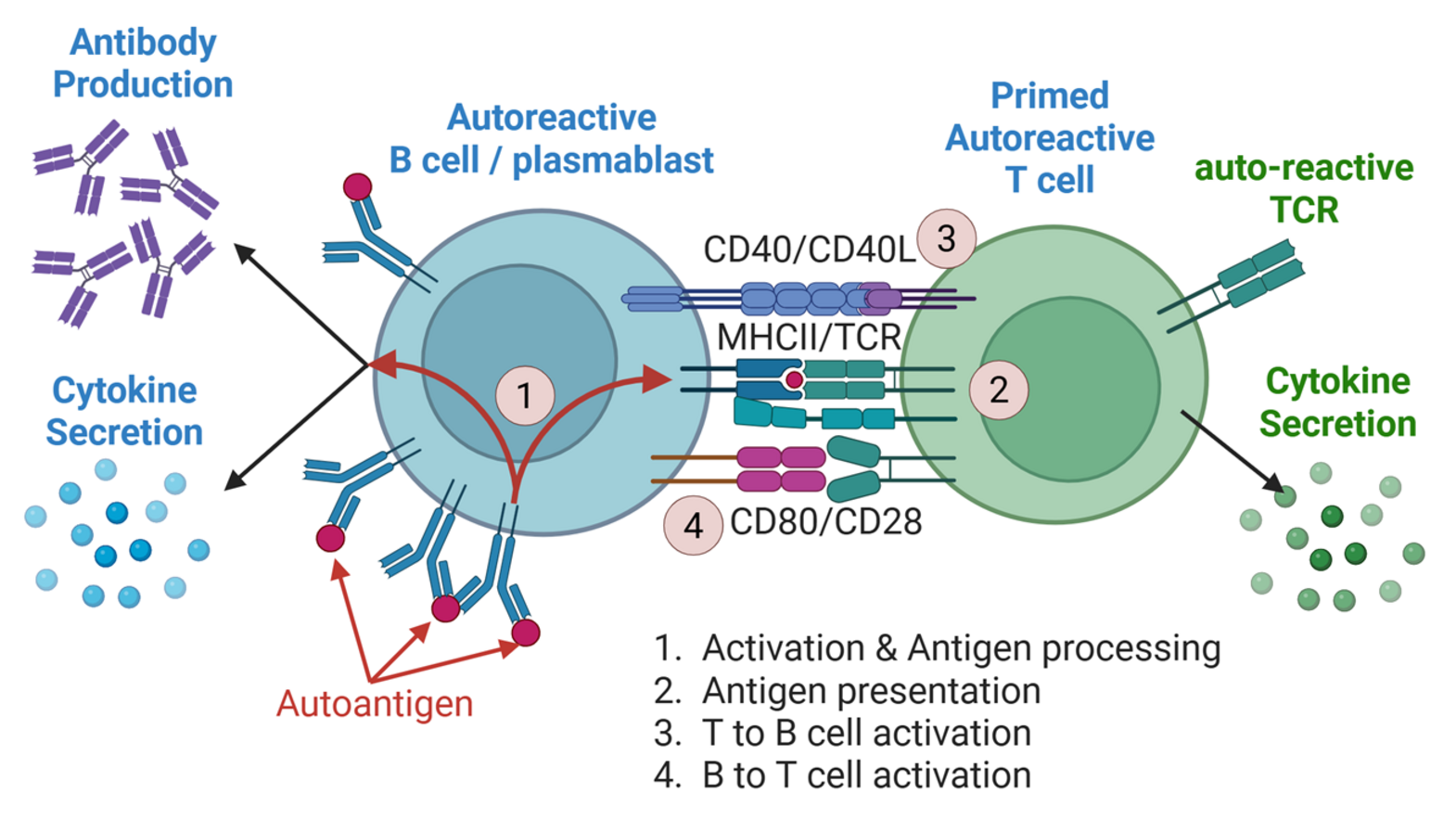
Abbildung:
Im Zentrum unserer Forschung steht das Verständnis des Crosstalks zwischen B-Zellen und T-Zellen sowie dessen Auswirkungen auf das Tumormikromilieu, Zelltherapien, systemische Entzündungsprozesse und die teils langfristigen Auswirkungen der Erkrankung auf das Immunsystem der Patientinnen und Patienten. Abbildung in Anlehnung an Müller, F. Innere Medizin 66, 810–817 (2025). Doi 10.1007/s00108-025-01945-x
Kollaborationen intern
- Prof. Dr. Metzler (Kinderklinik, Stellvertr. Direktor, Leiter der Onkologie)
- Prof. Dr. Nitschke (Biologie, Leiter des Lehrstuhls für Genetik)
- Prof. Dr. Christian Pilarsky (Chirurgie)
- Prof. Dr. Stürzl (Experimentelle Chirurgie, Leiter der Abteilung)
Kollaborationen extern
- Dr. Ira Pastan, National Institutes of Health, Bethesda, MD, USA
- Dr. Alan S. Wayne, Children's Hospital Los Angeles, CA, USA
- Medimmune, LLC, Gaithersburg, MD, USA
Ausgewählte Publikationen
George R, Gsottberger F, Ammon A, Wendland K, Mellenthin L, Mackensen A, Müller F. Triton X-114 and Amine-Based Wash Strategy Reduces Lipopolysaccharides to FDA Limit and Achieves Purer, More Potent Recombinant Immunotoxin. Bioconjug Chem. 2021 Apr 21;32(4):713-720. doi: 10.1021/acs.bioconjchem.1c00013. Epub 2021 Apr 1. PubMed PMID: 33793193.
Müller F, Cunningham T, Beers R, Bera TK, Wayne AS, Pastan I. Domain II of Pseudomonas Exotoxin Is Critical for Efficacy of Bolus Doses in a Xenograft Model of Acute Lymphoblastic Leukemia. Toxins (Basel). 2018 May 21;10(5). pii: E210.
Müller F, Cunningham T, Stookey S, Tai CH, Burkett S, Jailwala P, Stetler Stevenson M, Cam MC, Wayne AS, Pastan I. 5-Azacytidine prevents relapse and produces long-term complete remissions in leukemia xenografts treated with Moxetumomab pasudotox. Proc Natl Acad Sci U S A. 2018 Feb 20;115(8):E1867-E1875.
Müller F, Stookey S, Cunningham T, Pastan I. Paclitaxel synergizes with exposure time adjusted CD22-targeting immunotoxins against B-cell malignancies. Oncotarget. 2017 May 9;8(19):30644-30655.
Müller F, Cunningham T, Liu XF, Wayne AS, Pastan I. Wide Variability in the Time Required for Immunotoxins to Kill B Lineage Acute Lymphoblastic Leukemia Cells: Implications for Trial Design. Clin Cancer Res. 2016 Oct 1;22(19):4913-4922.
Liu X, Müller F, Wayne AS, Pastan I. Protein Kinase Inhibitor H89 Enhances the Activity of Pseudomonas Exotoxin A-Based Immunotoxins. Mol Cancer Ther. 2016 May;15(5):1053-62.
Hollevoet K, Mason-Osann E, Müller F, Pastan I. Methylation-associated partial down-regulation of mesothelin causes resistance to anti-mesothelin immunotoxins in a pancreatic cancer cell line. PLoS One. 2015 Mar 24;10(3):e0122462.
https://scholar.google.com/citations?user=o_TqNNUAAAAJ&hl=en